亞盛醫藥(06855)今日宣佈,公司已在第60屆美國臨牀腫瘤學會(ASCO)年會上,以壁報展示形式公佈了Bcl-2抑制劑APG-2575聯合阿扎胞苷(AZA)治療初治(TN)或復發/難治性(R/R)急性髓性白血病(AML)患者的Ib/II期臨牀研究的最新數據。
一年一度的ASCO年會是全球腫瘤領域最重要的、最爲權威的學術交流盛會,將展示當前國際最前沿的臨牀腫瘤學科研成果和腫瘤治療技術。今年是亞盛醫藥連續第七年亮相ASCO年會,作爲日益活躍在國際學術舞臺上的"中國聲音",此次公司共有3個原研品種的4項研究入選,其中1項獲口頭報告。
此次展示的APG-2575聯合AZA治療AML患者的臨牀研究數據體現了該聯合療法在老年/不耐受標準誘導化療的TN AML患者以及R/R AML患者中的卓越療效。此外,腫瘤溶解綜合徵(TLS)方面的安全性、較低的發熱性中性粒細胞減少發生率、以及較低的早期死亡率都展現出該聯合療法良好的安全性特徵。
金潔教授
該項臨牀研究的主要研究者
浙江大學醫學院附屬第一醫院
“APG-2575作爲具有完全獨立知識產權的新型Bcl-2抑制劑,反應率方面和國外同類產品相似,安全性顯示出明顯優勢。安全性優勢帶來的更少的治療相關死亡、更少的劑量調整、更及時的後續化療療程,有望對AML患者的長期生存產生促進作用。
王華鋒博士
該項臨牀研究的報告人
浙江大學醫學院附屬第一醫院
“Bcl-2抑制劑是AML治療領域的重要突破,但是國外同類產品的血液學安全性問題對Bcl-2抑制劑的臨牀廣泛應用和遠期療效方面存在不利影響。作爲本土創新藥物的優秀典範,APG-2575屢次在國際學術大會上發光發熱。APG-2575和化療聯合使用中,血液學不良反應的發生率較國外同類產品爲低;更關鍵的是,血液學不良反應程度輕,易於控制和處理。血液學毒性相關的其它嚴重事件如發熱性中性粒細胞減少、30d/60d內死亡率非常低,充分說明APG-2575的血液學毒性程度輕、持續時間短、嚴重程度低、易於控制且對後續化療療程的影響小。在安全性方面,APG-2575已經展現出優於國外同類產品的臨牀潛力。”
翟一帆博士
亞盛醫藥首席醫學官
“此次展示的APG-2575聯合AZA治療AML患者的療效和安全性數據令人欣喜,這不僅再次佐證了該品種的全球‘Best-in-class'潛力,也進一步表明APG-2575有望爲AML這一常見且預後極差的血液腫瘤領域帶來新的治療希望。值得一提的是,目前已有一項該品種治療AML患者的全球註冊III期臨牀正在開展,我們將堅守‘解決中國乃至全球患者尚未滿足的臨牀需求'這一使命,加快臨牀開發。期待在不遠的將來,APG-2575這一中國原創藥物能夠惠及廣泛的AML患者。”
在此次ASCO年會上展示的該臨牀研究核心要點如下:
Safety and efficacy of lisaftoclax, a novel BCL-2 inhibitor, in combination with azacitidine in patients with treatment-naïve or relapsed or refractory acute myeloid leukemia.
新型Bcl-2抑制劑APG-2575(Lisaftoclax)聯合阿扎胞苷治療初治或復發/難治急性髓性白血病患者的有效性和安全性
摘要編號:6541
分會場標題:血液腫瘤——白血病,骨髓增生異常綜合徵及異基因造血幹細胞移植(Hematologic Malignancies—Leukemia, Myelodysplastic Syndromes, and Allotransplant)
報告時間:
2024年6月3日星期一9:00 – 12:00(美國中部時間)
2024年6月3日星期一22:00 – 次日凌晨1:00(北京時間)
第一作者:王華鋒博士,浙江大學醫學院附屬第一醫院
核心要點:
研究背景和研究介紹:早期研究顯示,在AML中,APG-2575聯合多種藥物有協同誘導細胞凋亡的作用。本次會議報告一項探索APG-2575聯合AZA在成年AML患者中的安全性和有效性的Ib/II期研究的隨訪數據。
入組患者和研究方法:
該研究入組的患者爲老年(≥75歲)/不耐受標準誘導化療的TN AML患者,或R/R AML患者(≥18歲)。APG-2575每天口服一次(400/600/800mg),28天爲一個治療週期,在第一個治療週期中,APG-2575採用每日劑量遞增方案以預防TLS;75mg/m2的AZA於D1-7每天給藥一次。
截至2024年1月25日,已入組76例AML患者,其中37例爲R/R AML患者;39例爲老年/不耐受標準誘導化療的TN AML患者。中位年齡66歲(範圍,20-81)。
療效數據:
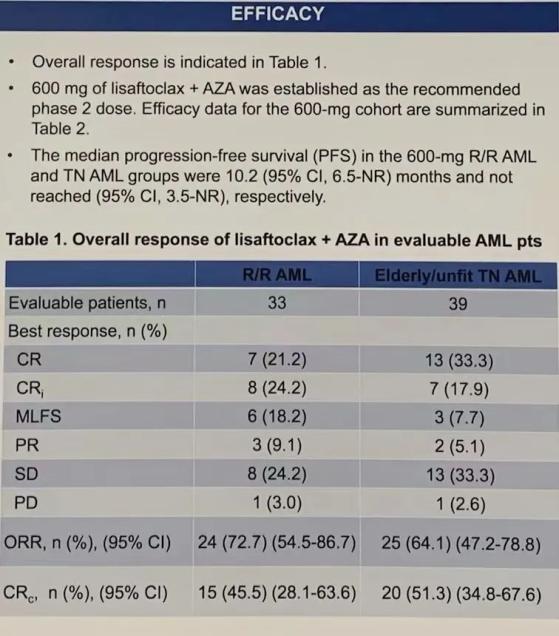
在所有經APG-2575聯合AZA治療的R/R AML患者中,總體反應率(ORR= CR + CRi + 形態學無白血病狀態[MLFS] + PR)爲72.7%,複合完全緩解率(CRc = CR+ CRi)爲45.5%。600mg劑量組(n=30)的中位治療持續時間爲3.8個月,ORR爲76.7%,CRc爲50.0%;達到CRc的中位時間爲2.5個月;中位PFS爲10.2個月;中位總體生存期(OS)爲14.7個月。
所有經APG-2575聯合AZA治療的TN AML患者中,ORR爲 64.1%,CRc爲 51.3%。600mg劑量組(n=29)的中位治療持續時間爲3.3個月;達到CRc的中位時間爲1.9個月;尚未達到中位PFS和中位OS。
600mg APG-2575被選定爲聯合AZA治療AML的II期研究推薦劑量(RP2D)。
安全性數據:所有患者均經歷了治療期間出現的不良事件(TEAEs),其中3/4級TEAEs發生率爲89.5%,嚴重不良事件(SAEs)發生率爲43.4%。常見的(≥10%)3級及以上的TEAEs包括中性粒細胞減少(57.9%)、血小板減少(50.0%)、貧血(27.6%)、肺炎(17.1%)和中性粒細胞減少伴發熱(10.5%)。未報道任何TLS事件。30天死亡率爲1.3%。
結論:本研究數據體現了新型Bcl-2抑制劑APG-2575聯合AZA在老年/不耐受標準誘導化療的TN AML患者以及R/R AML患者中的潛力,特別是展示了TLS方面的安全性、中性粒細胞減少伴發熱發生率較低,以及較低的早期死亡率。目前已有一項隨機雙盲的III期研究正在開展,將進一步探索APG-2575聯合AZA在老年/不耐受標準誘導化療的AML患者中的生存獲益。
本文轉載自“亞盛醫藥”微信公衆號,智通財經編輯:劉家殷。