教育和醫療是人類最不得不為的兩項事業,前者給予希望,後者確保了生存的基本權利。
隨著醫療保健意識的不斷提高,在政府政策及研發資金投入顯著增長的大力推動下,中國的生物製藥市場經歷著迅猛增長。
中國領先的生物製藥公司復宏漢霖-B(02696-HK)今天在香港交易所主板正式掛牌上市,此次上市為沉寂已久的香港資本市場帶來了一抹亮麗的色彩,為投資者提供了一個參與到這個蓬勃發展的產業的機會。
致力於為全球患者提供質高價優的創新生物藥,復宏漢霖此次計劃全球發售6469.54萬股,其中香港公開發售部分佔一成,國際配售佔九成,發售價定為49.60港元,擬籌30.963億港元(扣除費用後),主要用於核心產品、候選生物類似藥、生物創新藥的臨床試驗、監管備案及註冊,以及一般營運開支,聯席保薦人包括中金公司、美銀美林、招銀國際、復星恒利和花旗。香港公開發售和國際發售均獲適度超額認購。
類似藥+創新藥+聯合療法的多元化產品管線
主要專注於單抗生物藥開發的復宏漢霖擁有一個多元化的、領先的產品管線。從生物類似藥起步,復宏漢霖逐步開發創新型單抗產品,結合自主開發的抗PD-1和PD-L1單抗,在國内率先推出免疫聯合療法,把握未來腫瘤免疫機遇,提供可負擔的、療效更好的治療方案。
類似藥:可負擔的創新
復宏漢霖是首家根據現行中國有關生物類似藥評價及上市審批的法規《生物類似藥指導原則》開發和獲得國家藥監局新藥藥證申請批準的生物製藥公司,而且也是中國首家商業化推出生物類似藥產品的生物製藥公司。
2019年5月,復宏漢霖首款產品HLX01漢利康(利妥昔單抗注射液)正式上市銷售,主要用於治療非霍奇金淋巴瘤,首張處方已於2019年5月16日開出。利妥昔單抗已納入2019年8月20日頒佈的最新版國家醫保目錄,目前在若幹省份的定價低至1398元。據悉,HLX01擁有絕對的先發優勢,較後續競爭者大概提前了18個月。
注射用曲妥珠單抗HLX02可用於治療乳腺癌,是國内首個按照《生物類似藥研發與評價技術指導原則(施行)》進行研發,並且在中國、波蘭、烏克蘭及菲律賓開展全球3期臨床試驗的曲妥珠單抗,在全球範圍内擁有廣闊的市場前景。其已於2019年4月和2019年6月分别獲得國家藥監局和歐洲藥品管理局新藥藥證申請受理,現正由國家藥監局進行優先評審,是首個獲得新藥上市申請受理的國產曲妥珠單抗。
據估計,HLX02在中國有望達到100億人民幣的市場規模,復宏漢霖同時還通過國際化戰略合作,助力HLX02海外市場業務的開拓。2017年,復宏漢霖與雅各臣藥業達成合作協議,授予其關於HLX02在中國香港、中國澳門地區獨家開發和商業化行為授權及在部分東盟國家的優先談判權。此外,與Accord訂立在歐洲、中東-北非及獨聯體等70多個司法權區及地區的獨家商業權利。還於2018年6月與Cipla訂立在澳紐、哥倫比亞及馬來西亞的HLX02獨家許可及商業化權利。
先發優勢、更高的可及性以及高效質控下的產品質量優勢,這僅僅是復宏漢霖的其中幾項優勢,前邊我們提到,復宏漢霖的定價也極具競爭力,這是因為公司能夠按照國際GMP質量標準大規模生產,同時合理控制成本,通過運用及開發技術採取合理的成本控制措施,例如該公司已應用高表達的細胞株和自主細胞培養基進行HLX01(漢利康)的生產,並採用一次性生產技術。另外,其内部對從藥物研發到生產的每個流程進行端對端控制,以最大限度地降低外包成本。
創新藥:利用強大而全面的研發實力,推進生物創新藥的開發
憑借生物類似藥的奠基,復宏漢霖累積研發實力,開發生物創新藥。以其自主研發的創新型單克隆抗體項目HLX10(抗PD-1單抗)為例,該產品已相繼獲得美國、中國台灣及中國大陸的臨床試驗批準,可用於多種實體瘤的治療,單藥已經進入2期臨床試驗階段。
值得注意的是,復宏漢霖擁有全面的生物創新藥管線,除了PD-1抑制劑HLX10外,該公司的候選生物創新藥還包括新型PD-L1抑制劑HLX20、HLX06、HLX07、HLX22、HLX55、HLX09、HLX23、HLX53以及HLX24等。
基於自有產品的多元化聯合療法組合:把握未來腫瘤免疫機遇
癌症有人類「頭號殺手」之稱,因此研發抗癌藥成為人類孜孜不倦改變命運的探索。
癌症是人體細胞「變壞」所致,人體的免疫係統有一種T細胞白血球能夠吞噬這些「壞細胞」,但是為了避免T細胞白血球「濫殺」「好細胞」,T細胞白血球上有一個被稱為PD-1的「開關」,能夠關閉T細胞白血球的吞噬功能。癌細胞針對這個弱點,分泌名叫「PD-L1」的蛋白質,關閉PD-1,也就關閉T細胞的吞噬功能。PD-1/PD-L1免疫療法就是通過藥物「關閉」PD-1與PD-L1的聯通,從而讓人體自身的免疫係統能夠攻擊腫瘤細胞。目前,可以通過PD-1抑制劑和PD-L1抑制劑,前者讓T細胞繼續殺滅癌細胞,後者阻止PD-L1發揮功能,來保障T細胞的吞噬功能順利運行。
然而,抗PD-1產品作為單藥使用有效率較低,為了改善這個情況,在單藥基礎上開發聯合療法已成為全球趨勢。復宏漢霖在國内率先推出免疫聯合療法。
目前,復宏漢霖已陸續就HLX10與自有產品HLX04、HLX07等單抗以及化療聯用開展多項腫瘤免疫聯合療法,覆蓋多種癌症的治療,包括頭頸部鱗狀細胞癌、局部晚期/轉移性食管鱗癌、局部晚期/轉移性鱗狀非小細胞肺癌、廣泛期小細胞肺癌、轉移性非鱗狀非小細胞肺癌以及肝細胞癌等。
值得注意的是,復宏漢霖踐行的「Global + Combo」差異化戰略,以HLX10為核心的聯合療法在全球多個國家和地區同步開展臨床試驗,這將有效加速其腫瘤免疫聯合療法戰略的進一步落地。
事實上在不久之前,復宏漢霖宣佈與東南亞規模最大的上市醫藥公司之一Kalbe Farma旗下控股子公司KG Bio達成合作共識,授予KG Bio就復宏漢霖自主研發HLX10的首個單藥療法及兩項聯合療法在東南亞10個國家的獨家開發和商業化權利,而KG Bio將向復宏漢霖支付合計金額6.92億美元。通過此次合作,復宏漢霖將可借助合作夥伴在海外的大規模業務網絡,加快其產品的國際化進程,進一步提升復宏漢霖在腫瘤免疫治療領域的品牌知名度和國際市場競爭力。
具成本效益與健全質管體係的大規模生產能力+高效的一體化全球研發平台
復宏漢霖在上海建成生產單克隆抗體產品的徐匯基地,產能14000升,有六台2,000升一次性生物反應器及四台500升一次性生物反應器,該生產基地已通過歐盟質量受權人(QP)檢查,具備了GMP認證的生產能力。與此同時,該公司正在上海松江建設一座大型的生物藥產業化基地,該基地嚴格按照國際GMP標準設計,充分應用一次性生產技術等國際先進技術,滿足生物醫藥自動化、信息化、智能化國際水平,成為低碳、節能、環保的現代化智能生物醫藥基地。
復宏漢霖在中國上海、中國台北和美國加州設有三個研發基地,在上海的研發基地側重研發的後期階段,能迅速把握商業規模生產的機遇。台北和加州研發中心則主要負責早期研發,其中台北研發中心主要負責以候選藥物篩選為重點的先導藥物開發、優化、及新藥臨床註冊和試驗,運用各種動物藥效模型分析生物體内的藥物學;加州研發中心則快速了解把握單抗領域的最新發展及尖端技術,主要負責以細胞株構建、篩選等為重點的藥物早期開發階段。
上市的里程碑意義
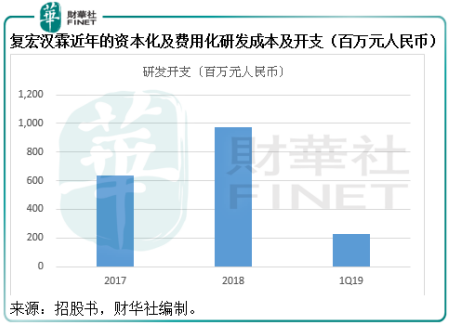
從生物類似藥起步,逐步開發創新型單抗產品,結合自主開發的抗PD-1和PD-L1單抗,在國内率先推出免疫聯合療法,前瞻性佈局一個多元化、創新單抗及腫瘤免疫聯合療法管線,復宏漢霖在生物類似藥持續開發方面享有先發優勢,在創新藥方面也有無可比擬的技術實力,同時率先開發和推進聯合療法,拓展研發管線。在過去幾年,復宏漢霖不斷加大研發的投入力度,2019年第一季,其包含資本化及費用化成本在内的資本開支達到2.254億元人民幣,同比增長1.01倍,而該公司也計劃通過上市籌資,為未來的研發工作補充彈藥。
復宏漢霖擁有強大的研發實力和符合國際質量標準的生產設施,與此同時,實力雄厚的母公司復星醫藥提供了豐富的資源、市場準入、全國性的銷售及市場網絡。復宏漢霖將可憑借母公司的支持和協同效應快速實現其產品的大規模商業化。復宏漢霖自身生物藥全產業平台的核心能力加上在港交所上市的品牌宣傳效力,上市僅僅是其漫長行進路的第一步,期待這家創新藥企質的飛躍。