科濟藥業(02171)8月23日公布了2021年上半年度業績。
上半年,該公司全球化布局取得了諸多成果,例如CT053順利進入美國臨床II期試驗,是少數進入該階段的中國藥企自主研發的CAR-T産品;今年7月,該公司首次完成兩款CAR-T候選産品對外授權,成功開啓國際化合作;美國生産設施獲得當地政府批准啓動建設,自有産能加速落地。
科濟藥業創始人、董事會主席、首席執行官、首席科學官李宗海表示:“這是科濟藥業繼2021年6月18日在香港交易所成功上市後的第一個中期業績報告。2021年上半年,科濟藥業在全社會各方的鼎力支持下,在産品管線推進、技術開發、對外合作、生産設施建設等方面取得多項重要進展。科濟將一如既往地努力在全球範圍內推進臨床候選産品,持續開發自主創新技術,爲全球癌症患者帶來更多創新和差異化的細胞療法,也爲廣大投資者和社會創造更多價值”
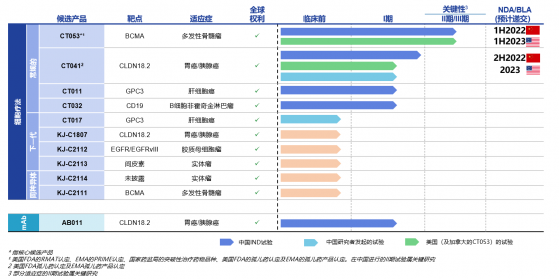
作爲CAR-T細胞療法領域的主要參與者,科濟藥業自主開發了11款差異化候選産品,並擁有全球權益。
其中CT053作爲升級版靶向B細胞成熟抗原(「BCMA」)的全人抗CAR-T産品,正在中國進行關鍵II期臨床試驗;2021年7月,CT053美國關鍵II期臨床試驗入組第一例患者。該公司計劃于2022年上半年就CT053向中國國家藥監局(NMPA)提交新藥上市申請(NDA),並計劃在2023年上半年向美國FDA提交生物制品上市申請(BLA)。根據科濟藥業公開資料顯示,在中國進行的研究者發起的試驗、以及中國和北美進行的注冊臨床試驗中,顯示出令人鼓舞的療效和安全性。
另一款CT041爲全球唯一靶向CLDN18.2的且已獲得美國FDA和國家藥監局的IND批准並正在進行臨床試驗研究的CAR-T候選産品,用于治療胃癌和胰腺癌等實體瘤,已獲得FDA及EMA孤兒藥産品認定。有望實現CAR-T療法在實體瘤治療領域的突破。科濟藥業將于9月19日ESMO大會上對CT041 中國研究者發起試驗(IIT)數據進展進行口頭報告。此外,2021年上半年,科濟藥業已在中國向NMPA提交關鍵II期研究的咨詢申請,並計劃于2021年下半年啓動關鍵II期臨床試驗,2022年下半年就先前至少接受兩線系統治療失敗的胃癌患者的治療提交NDA。在美國,公司計劃于2022年對胃癌╱食管胃結合部癌或胰腺癌患者進行關鍵的II期試驗,2023年向美國FDA提交BLA。CT041已獲得美國FDA授予「孤兒藥」認定,用于治療胃癌/胃食管結合部癌,並獲得EMA授予「孤兒藥産品」認定,用于治療胃癌。
根據科濟藥業中期業績報告顯示,科濟藥業旗下公司CAFA therapeutics與韓國HK inno.N (KOSDAQ: 195940)公司就人源化CD19 CAR-T(CT032)和全人抗BCMA CAR-T(CT053)兩款細胞療法産品進行開發和商業化達成許可及協議。根據協議條款,科濟藥業有權獲得的預付款和額外的裏程碑付款總計達5000萬美元,科濟藥業還將有資格獲得基于合作約定産品在韓國未來淨銷售額至多兩位數百分比的特許權使用費。
此次對外授權合作是海外市場對科濟藥業CAR-T産品的肯定,也爲該公司未來在全球範圍內展開更多産品和技術合作打開了良好開端。
目前該公司擁有11款候選産品,均爲自主研發且擁有全球權益,涵蓋常規型、新一代CAR-T 技術及同種異體療法,布局全面且富有前瞻性。
此外,本次中期業績發布,該公司透露,在現有産品管線基礎之上,科濟將圍繞“實體瘤療效、安全性、患者可及性、靶點可用性”四大研發戰略方向,持續開發創新專有技術 (CycloCAR, THANK-uCAR等), 以解決CAR-T療法領域的主要挑戰。例如針對實體瘤療效問題,公司正在開發下一代CAR-T技術CycloCAR,該技術共同表達細胞因子IL-7和趨化因子CCL21,可能具有更高的臨床療效,並減少對清淋化療預處理的要求。未來,這些技術平台也將爲臨床階段持續提供更多自主研發候選産品。
科濟藥業已在中國、美國和加拿大獲得7項CAR-T療法的IND許可,在中國所有CAR-T公司中排名第一。除了國際化的産品研發布局,該公司也在海外積極建設自有産能。
已經建立了符合GMP標准的內部制造能力,包括質粒、慢病毒載體和CAR-T細胞産品的端到端生産。位于中國上海金山區的商業化生産廠房,取得了中國第一張CAR-T細胞療法的藥品生産許可證,預計每年可支持多達2,000名患者的CAR-T治療。
2021年上半年,在美國北卡羅來納州達勒姆市,科濟藥業已啓動生産設施建設,用于臨床試驗和早期商業化的生産設施建設。
憑借豐富的自研産品管線、自有CAR-T産能及全球化市場布局,公司將持續提高CAR-T産品的生産規模效應,進一步降低每個患者的用藥成本,改善CAR-T療法可及性,最終爲全球癌症患者帶去創新、差異化、可負擔的的細胞療法。