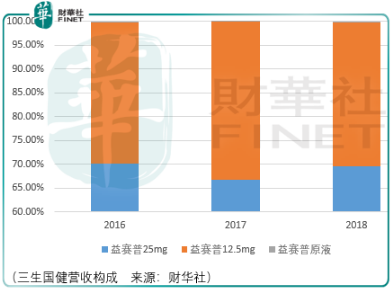
三生國健是一家專注抗體類藥物的創新型生物醫藥企業,目前核心的收入來源為重組人ii型tnf-α(腫瘤壞死因子)受體-抗體融合蛋白(商品名益賽普)。自研的重組抗CD25人源化單克隆抗體注射液於2019年6月獲得國家藥品監督管理局頒發的藥品 GMP證書,於2019年10月開始上市銷售。
此外,三生國健還擁有15個在研抗體藥物(7個處於臨床及臨床後階段的在研藥物、8個處於臨床前階段的在研藥物),其中大部分在研藥物為治療用生物製品1類或單克隆抗體,並包括1個中美雙報的在研藥物、1個被納入優先審批的在研藥物。
益賽普
益賽普於2005年上市,是國内首個上市的全人源抗體類藥物、中國風濕病領域第一個上市的腫瘤壞死因子(tnf-α)抑制劑,可用於治療類風濕關節炎、強直性脊柱炎、銀屑病。
腫瘤壞死因子-α(TNF-α)是主要由巨噬細胞和單核細胞產生的一種促炎細胞因子,屬於引起急相反應的眾多細胞因子中的一員,主要作用是調節免疫細胞的功能。TNF-α 作為一種内源性致熱原,能夠促使發熱、引起細胞凋亡並導致炎症等症狀。目前,多項臨床研究已證明 TNF-α 在多種疾病(如自身免疫病、休克、變態反應等)中高表達,產生促進炎症和組織損傷的病理效應,與諸如類風濕關節炎(RA)、強直性脊柱炎(AS)、銀屑病(PS)、克羅恩病(CD)等自身免疫性疾病的發病密切相關。
TNF-α 抑制劑是以一類以TNF-α為靶點的生物製劑,例如融合蛋白和單克隆抗體,它可以阻止 TNF-α 與 TNF 受體的結合,阻斷其下遊信號的轉導通路,從而阻止炎症反應的發生。
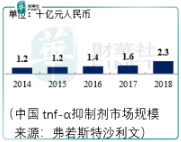
中國TNF-α抑制劑市場目前由 8 款生物藥組成,是中國自身免疫性疾病生物藥市場的重要組成,2018 年佔中國自身免疫性疾病生物藥市場的份額約 93.6%,根據弗若斯特沙利文報告,2018 年益賽普在國内TNF-α 抑制劑市場的份額約 52.3%。
從針對適應症的數量比對來看,強生的類克比益賽普要多一個適應症cd(crohn’s disease克羅恩病),同時國内獲批時間上僅晚1年,這說明益賽普在針對ra(類風濕關節炎)、as(強直性脊柱炎)、ps(銀屑病)適應症的藥效不僅要優於類克,還要優於其餘較晚獲批上市的tnf-α抑制劑。
因此,即便截至2019年9月底,中國tnf-α抑制劑提交上市申請和處於臨床iii期階段的產品分别達到6個和7個,也不能說明這些藥企就能重新搶走三生國健的市場。同時,三生國健亦在豐富自身tnf-α抑制劑的產品組合,其重組人ii型tnf-α受體-抗體融合蛋白預充式注射液目前處於nda(新藥提交申請上市)階段,適應症為ra、as、ps,作為中國首個提價nda自主研發預充式融合蛋白注射液的廠商,其該領域的產品將有望繼續保持甚至增加其市場份額。
伊尼妥單抗
三生國健研發的注射重組抗her2單抗目前處於nda階段,其作用原理為抗HER2單克隆抗體通過將自身附著在her2上來阻止人體表皮生長因子在her2上的附著,從而阻斷癌細胞的生長,並可以刺激人體自身的免疫細胞去摧毀癌細胞。
Her2稱為人類表皮生長因子受體,在許多腫瘤中均有表達,常見於乳腺癌、胃癌中。在中國臨床腫瘤學會發佈的《乳腺癌診療指南》中,曲妥珠單抗聯合化療被推薦為her2陽性乳腺癌術前治療方案(I 級推薦)、her2陽性早期乳腺癌術後輔助靶向治療(I 級推薦)以及 her2陽性晚期(復發轉移)乳腺癌的抗her2一線和二線治療方案(I 級推薦);根據《胃癌 her2檢測指南(2016 版)》的研究顯示,中國胃癌患者her2陽性率約 13%。在中國臨床腫瘤學會發佈的《胃癌診療指南》中,曲妥珠單抗聯合化療被推薦為her2陽性晚期轉移性胃癌一線治療方案(I 級推薦)。
根據nmpa(國家藥品監督管理局)數據,截至2019年9月30日,中國一共有 2款已上市的抗her2單抗,分别是羅氏的曲妥珠單抗(赫賽汀)和羅氏的的帕妥珠單抗(帕捷特),其中赫賽汀於2002年在中國獲批上市,獲批適應症包括her2陽性早期/轉移性乳腺癌和 her2陽性轉移性胃癌,並進入2019年國家醫保目錄乙類;帕捷特於2018年在中國獲批上市,獲批適應症為與曲妥珠單抗和化療聯合作為具有高復發風險her2陽性早期乳腺癌患者的輔助治療。
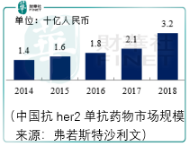
雖然國内抗her2單抗藥物市場空間足夠大,復合增速足夠亮眼,但顯然這一領域的先發者是羅氏而非三生國健,三生國健產的伊尼妥單抗未來是否具備替代羅氏赫賽汀和帕捷特存在較大的不確定性。同時,除了與羅氏競爭之外,截至 2019年9月30日,中國抗her2單抗提交上市申請(nda)和處於臨床III期階段的產品分别為2個(另一個為復宏漢霖的曲妥珠單抗)與6個,也就是說三生國健的伊尼妥單抗還需要與復宏漢霖、嘉和生物、海正藥業等廠家所生產的同類藥品進行競爭,前景究竟如何,需要企業給出進一步的數據才能判斷。
健尼哌
健尼哌為重組抗 CD25人源化單克隆抗體注射液的商品名,該藥品為三生國健自主研發,是目前國内唯一獲批上市的人源化抗 CD25單抗,已於2019年6月獲得國家藥品監督管理局頒發的藥品 GMP證書,並於2019年10月開始上市銷售。
健尼哌可用於預防腎移植引起的急性排斥反應,可與常規免疫抑制方案聯用,能顯著提高移植器官存活率,改善患者生存質量。
根據 nmpa數據,截至2019年9月30日,中國一共有 2款抗 CD25 單抗獲批上市,分别是諾華的巴利昔單抗(舒萊)和三生國健的重組抗CD25人源化單抗(健尼哌)。其中:舒萊於 2002 年在中國獲批上市,目前獲批的適應症為預防腎移植術後的早期急性器官排斥,並進入 2019 年國家醫保目錄乙類。
2014-2018年間,舒萊的營收從0.7億元增長至1.3億元,這意味著對於2018年營收就有11.42億元的三生國健,健尼哌未來的潛在收入貢獻對其成長增速影響不大,因此投資者應當把注意力放在伊尼妥單抗潛在的收入增長上。
總結
總體而言,益賽普作為三生國健的業務基石,儘管預期其市場份額被蠶食的風險並不大,但仍然需要注意其市場份額的變化情況。總體業務估值彈性上則主要取決於伊尼妥單抗市場份額的提升情況,其是否具備挑戰羅氏的能力需要進一步的數據進行確認。在此之前,投資者不妨對三生國健報以樂觀期待,等到靴子落地,或許就是階段獲利為安之時。
