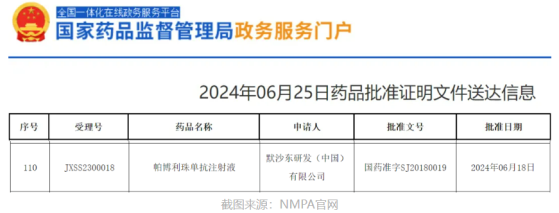
智通財經APP獲悉,6月25日,中國國家藥監局(NMPA)官網公示,默沙東(MRK.US)的抗PD-1單抗帕博利珠單抗又一項新適應症上市申請獲得批准。根據默沙東新聞稿,該藥本次獲批的適應症爲:聯合曲妥珠單抗、含氟尿嘧啶類和鉑類藥物化療,用於經充分驗證的檢測評估腫瘤表達PD-L1(CPS≥1)的局部晚期不可切除或轉移性HER2陽性胃或胃食管結合部腺癌患者的一線治療。至此,帕博利珠單抗在中國獲批的適應證已經達到14個。
據悉,此次帕博利珠單抗新適應證的獲批是基於全球3期臨牀研究KEYNOTE-811的數據。據默沙東公開資料介紹,KEYNOTE-811是一項隨機雙盲3期試驗,招募了約732名患者。雙主要終點是盲態獨立中心審評根據RECIST v1.1評估的無進展生存期(PFS)和總生存期(OS)。次要終點包括客觀緩解率(ORR)、緩解持續時間和安全性。
2023年,著名醫學期刊《柳葉刀》上發表的中期分析結果顯示KEYNOTE-811研究達到其中一個主要終點——顯著延長患者的PFS。在中位隨訪時間爲約28個月時,帕博利珠單抗組合療法組的PFS爲10個月,僅接受曲妥珠單抗和化療治療的患者組這一數值爲8.1個月。添加帕博利珠單抗將患者疾病進展或死亡風險降低28%。
今年5月,默沙東宣佈KEYNOTE-811中達到另一個主要終點,可顯著延長患者的OS。據悉,這一積極數據有望支持帕博利珠單抗將FDA的加速批准轉化爲完全批准。
據默沙東全球高級副總裁兼中國研發中心總裁李正卿博士介紹,近十年來,HER2陽性晚期胃癌一線治療領域鮮有新的治療方案出現。去年,帕博利珠單抗已經在中國境內獲批聯合化療用於局部晚期不可切除或轉移性HER2陰性胃或胃食管結合部腺癌患者的一線治療,此次獲批則將進一步爲PD-L1表達陽性(CPS≥1)的HER2陽性胃癌患者人羣帶來個性化治療方案。