隨着政策措施陸續出臺及資源配置不斷優化,國內生物醫藥產業正步入全面發展的關鍵階段。近日,市場流出的一份關於“全鏈條支持創新藥”的政策文件更是爲創新藥未來發展及市場投資點燃一盞明燈。而這對於一直堅持差異化創新研發的德琪醫藥來說,無疑是一個巨大利好。
當前國內創新藥前沿發展已不再是單純的Me-too/Me-better,而是已經轉型更高端的Best/First-in-class。而通過打造具有前瞻性、差異化的研發戰略和豐富管線儲備,持續構造國際化“同類首創”和“同類最優”競爭優勢,德琪醫藥-B(06996)已然走在創新藥趨勢發展的最前沿,內在價值逐步得到釋放。
另一方面,在全球生物醫藥融資環境還未明朗的當下,成熟的創新研發體系、完善的國際開發能力和充沛現金流,也成爲德琪醫藥構築穩健基本盤的關鍵基礎。因此,解構德琪醫藥新出爐的2023年財報,投資者可以從差異化創新管線研發、國際商業化合作與市場推進以及現金流等多維度,加深對公司核心競爭力以及中長期價值走向的認知與理解。
差異化創新研發即將來到集中爆發關鍵年
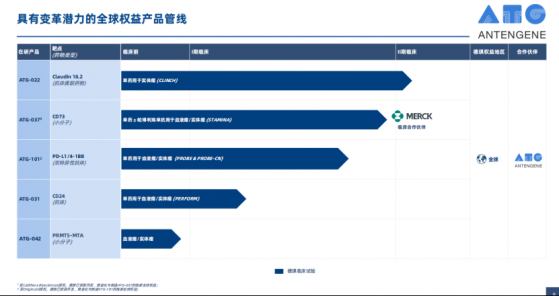
智通財經APP瞭解到,2024年將是德琪醫藥差異化創新研發取得重要進展的關鍵年份。因此,透過財報數據看公司管線研發的推進,能讓投資者對公司即將到來的跨越式發展有更清晰的認知。財報顯示,德琪醫藥建立了一條具有全球競爭力的“同類最優”或“全球首創”潛力的創新腫瘤免疫研發管線,並與全球超過100個臨牀機構進行合作,推進多個產品的全球化臨牀開發。全面的管線設置和廣泛的臨牀開發,彰顯了德琪醫藥從biotech向上升級的決心。
例如在臨牀前管線中,德琪早期研發團隊自主開發了一款新型“2+1”T細胞銜接器平臺AnTenGagerTM,其採用平衡性的CD3抗體親和力,具有靶點依賴性的激活作用,數據顯示具有更好療效和安全性。此外,AnTenGagerTM的多個分子顯示更強勁的腫瘤殺傷活性,同時具有更低的細胞因子釋放風險。與多種靶點的形成的雙特異抗體,有望在多種血液瘤或實體瘤治療中取得突破。
而在步入臨牀階段的研發管線中,德琪也佈局了不少高潛力前沿創新靶點。
以ATG-037爲例,其作爲小分子CD73抑制劑,在目前臨牀相關所有產品中具有最高的抑制活性。臨牀數據顯示,I期STAMINA研究爬坡階段有12例既往接受過檢查點抑制劑(CPI,帕博利珠單抗或納武利尤單抗)治療的患者在接受了至少2個週期的ATG-037單藥後接受聯合帕博利珠單抗的治療,其中有7例患者仍在接受治療。研究中,有2例黑色素瘤的患者(既往接受過抗PD-1抗體治療)和1例既往接受過化療聯合CPI(抗PD-1抗體)治療的非小細胞肺癌(NSCLC)患者達到部分緩解(PR)。
在PD-L1/4-1BB雙特異性抗體領域,德琪則開發了一款具備BIC潛力的ATG-101,其僅可在PD-L1交聯條件下激活4-1BB表達陽性的T細胞,這讓ATG-101具有較同靶點競品的肝臟毒性更低,且能有效抑制ICI耐藥腫瘤生長。研究數據也顯示,該藥具備良好的安全性且無顯著肝臟毒性。
在當前全球熱門的ADC賽道,德琪醫藥同樣頗有建樹。其旗下的Claudin 18.2抗體偶聯藥物ATG-022在CLDN18.2高表達和低表達的模型中顯示了極高的劑量依賴的體內活性。對比目前國內多家處在臨牀階段的CLDN18.2 ADC產品,ATG-022具備一定的同類最佳潛質。
繼CD47後,另一個具備“別喫我信號”的靶點CD24近年來受到國際學界廣泛關注。與CD47相比,CD24在腫瘤細胞表面表現出更高的表達量,同時其更窄的正常組織表達也預示着該靶點存在更大的治療窗口。
作爲德琪旗下的CD24單抗產品,AGT-031在去年5月獲批臨牀試驗,成爲美國首款進入腫瘤臨牀研究的抗CD24單克隆抗體藥物,研發進度走在全球前列。目前,ATG-031已完成I期臨牀研究的首個劑量水平隊列,展現出良好的安全性和耐受性,5例患者中均未觀察到劑量限制毒性(DLT),1例既往接受過7線治療的患者已獲得影像學確認的腫瘤體積縮小。
據智通財經APP瞭解,目前德琪醫藥的中後期臨牀資產進展也在如火如荼地推進中,例如目前正在順利開展中的ATG-008(雙重mTORC 1/2抑制劑)的II期TORCH-2概念性驗證研究,以及4項塞利尼索的關鍵性研究。其中,ATG-008作爲新一代mTORC抑制劑,在聯合特瑞普利單抗(抗PD-1抗體)治療復發/轉移性宮頸癌方面,相較現有的標準治療藥物數據已顯示出更爲突出的療效。
此外,德琪醫藥四項前沿研究成果還將在今年AACR年會上集體亮相。屆時,公司將首次公佈ATG-022(Claudin 18.2抗體偶聯藥物)伴隨診斷抗體的研究成果,並公佈MTAPnull選擇性小分子PRMT5抑制劑ATG-042的首篇臨牀前摘要以及自研T細胞銜接器平臺AnTenGagerTM和LILRB4xCD3 T細胞銜接器ATG-102的最新數據。以上充分印證了國際學術界對德琪醫藥強勁研發實力和硬核創新價值的高度認可。
挖掘核心品種市場潛力,穩步夯實公司基本盤
在“全鏈條支持創新藥”的政策風向下,創新藥企要想“謀發展”,則需堅持從患者的臨牀實際需求出發進行差異化創新。而不斷拓展商業化品種適應症市場並輔以商業化合作,則是實現“內外兼修”全面加速創新的重要途徑,德琪醫藥顯然深諳此道。
據智通財經APP瞭解,作爲全球首個全新機制的口服選擇性核輸出蛋白(XPO1)抑制劑,德琪的商業化核心品種希維奧®通過抑制核輸出蛋白XPO1,可促使腫瘤抑制蛋白和其他生長調節蛋白的核內儲留和活化,並下調細胞漿內多種致癌蛋白水平,體現出顯著的差異化創新水平和治療潛力。
爲滿足更廣闊的患者需求,去年8月11日,德琪醫藥就希維奧®(塞利尼索)在中國大陸商業化與翰森製藥達成超7億元商業化合作。在雙方合作下,希維奧®在國內醫院覆蓋和市場滲透方面有望進一步加速。
值得一提的是,去年12月14日,德琪醫藥正式宣佈希維奧®獲納入最新的國家醫保目錄名單。希維奧®作爲具有高臨牀價值的品種進入醫保後未來有望實現進一步的銷售放量。
與此同時,德琪也在加速全球市場開發,以期將希維奧®覆蓋更多的全球患者。目前,希維奧®已在全球42個國家和地區獲批上市,其中包括中國大陸、中國臺灣、中國香港、中國澳門、韓國、新加坡和澳大利亞。
除此之外,基於其獨特的作用機制,德琪醫藥也在持續爲希維奧®拓展適應症市場,開發針對希維奧®在瀰漫性大B細胞淋巴瘤(DLBCL)、T細胞非霍奇金淋巴瘤(T-NHL)和骨髓纖維化(MF)等不同疾病領域的多種聯合療法,並已有顯著成效。
以最常見的非霍奇金淋巴瘤類型DLBCL爲例,數據顯示,目前在中國和全球分別有超過20萬和近100萬DLBCL存量患者,並且全球每年約有15萬人被確診,其市場空間不亞於SLL/CLL。此前機構預測,到2030年,中國DLBCL藥物市場規模將達到369億元。
據悉,德琪醫藥已向NMPA提交希維奧®用於治療既往接受過至少兩線治療的復發/難治性瀰漫性大B細胞淋巴瘤 (R/R DLBCL)成人患者的新藥補充申請(sNDA)。若未來新適應症在國內順利獲批,該品種有望惠及更多的未滿足治療需求的患者,並增厚公司的收入和利潤。
其實,加快核心產品適應症拓展及商業化合作,也在側面顯示出德琪醫藥正在儲備充足的“糧草”,不斷提升自身“造血能力”。財報顯示,2023年公司現金及銀行結餘達11.88億元,穩健的現金流無疑是當下公司穩定估值和企業發展的關鍵基石。不過德琪當前的總市值,僅僅7.63億港幣,仍低於其現金價值。另外,當前德琪每股淨資產已達到2.36港元,高於其實際股價,公司整體估值處在明顯低估狀態。
從上述分析不難看出,德琪醫藥的創新研發即將來到集中爆發期,隨着未來公司差異化研發管線產品陸續落地,公司內在價值將不斷釋放,而這也將成爲其股價和公司估值反彈最重要的催化劑。