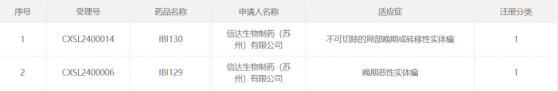
智通財經APP獲悉,3月19日,中國國家藥監局藥品審評中心(CDE)官網公示,信達生物(01801)開發的IBI130獲批臨牀,擬開發用於不可切除的局部晚期或轉移性實體瘤。而在幾日前(3月13日),該公司開發的IBI129也剛在中國獲批臨牀,擬開發用於治療晚期惡性實體瘤。
根據信達生物官網信息,IBI130是一款靶向TROP2的抗體偶聯藥物(ADC),IBI129是一款靶向B7-H3的ADC。據瞭解,目前,IBI129已進入到1期臨牀試驗階段。根據中國臨牀試驗登記與信息公示平臺,信達生物已於日前登記了一項國際多中心1/2期臨牀試驗,旨在評估IBI129治療局部晚期不可切除或轉移性實體瘤受試者的安全性、耐受性和有效性。該研究計劃在中國境內入組342例患者,國際上入組362例患者。
值得一提的是,針對B7-H3靶點,信達生物開發了多款藥物。除了靶向B7-H3的ADC產品IBI129,該公司還開發了:IBI334,一種新型抗體依賴性細胞毒性(ADCC)增強的B7-H3/EGFR雙特異性抗體;IBI3001,一種靶向B7-H3和EGFR的雙特異性ADC。IBI334和IBI3001各有一項研究入選本屆2024年美國癌症研究協會(AACR)年會的Late-Breaking Research環節。