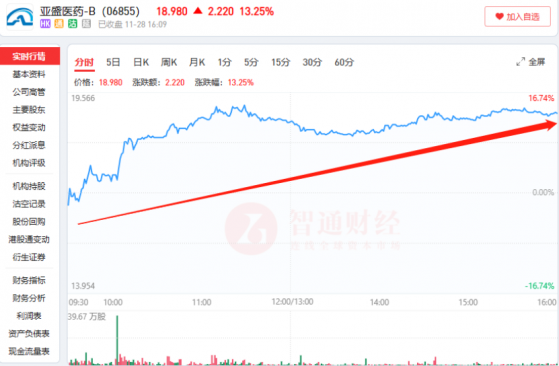
近日,港股醫療板塊迎來持續調整。恒生醫療保健指數和恒生醫療ETF(513060)持續波動下滑走低。然而亞盛醫藥-B(06855)股價卻一反板塊下跌頹勢,11月28日持續逆市上漲,最高達到19.20港元,最終收漲13.25%,領跑港股醫藥板塊。
轉型全産業鏈創新企業,提升市場信心
之所以亞盛醫藥這邊“風景獨好”,在于前一日公司發布公告,亞盛醫藥日前通過現場核查、並獲准核發藥品生産企業許可證(A證)。
智通財經APP了解到,該證爲2022年度蘇州市生物醫藥企業所獲取的首張A證類藥品生産許可證,也是江蘇省相關部門成立以來所獲取的首張A證類藥品生産許可證。
該産業基地按歐美和中國的cGMP要求完善並執行質量管理。該證的獲批將支持公司在蘇州生産具有全球專利和全球市場潛力的創新藥,並向全球市場供藥,充分體現了蘇州一號産業頭部標杆企業的強大發展後勁。顯然,這是繼2021年12月全球總部、研發中心在蘇州啓用後,亞盛醫藥迎來的又一重大裏程碑,也是公司從蘇州走向世界的嶄新起點。
據悉,亞盛醫藥全球産業基地位于亞盛醫藥全球總部園內,目前建成的口服固體制劑年産能爲2.5億片或膠囊,可滿足不同階段臨床樣品及商業化藥品的生産需求。
公司正在進行關鍵注冊臨床試驗的重磅産品Bcl-2選擇性抑制劑APG-2575片劑,後續將在該産業基地進行臨床樣品生産、注冊批和工藝驗證批生産以及未來的商業化生産。
值得一提的是,今年10月26日,亞盛醫藥正式向國家藥品監督管理局藥品審評中心(CDE)遞交新藥臨床試驗(IND)申請,計劃開展在研原創1類新藥APG-2575治療系統性紅斑狼瘡(SLE)的臨床研究,開啓非腫瘤領域探索。
而在血液腫瘤及實體瘤治療研究領域,APG-2575展現的Best-in-Class潛力同樣獲得國際學界高度認可。
11月3日,亞盛醫藥宣布,公司向第64屆美國血液學會(American Society of Hematology,ASH)年會遞交的4項臨床階段研究數據全部入選口頭報告,其中便包括APG-2575單藥或聯合治療初治、複發或難治(R/R)慢性淋巴細胞白血病/小淋巴細胞淋巴瘤(CLL/SLL)患者的全球II期臨床研究初步數據,該數據也是公司首次披露,備受國際業界和市場雙重期待。
作爲全球第二個、國內首個看到明確療效、並進入關鍵注冊臨床階段的Bcl-2抑制劑,APG-2575在此次ASH年會口頭報告的數據體現了該品種在R/R CLL/SLL患者中強勁的單藥和聯合治療潛力。
顯然,隨着APG-2575在腫瘤及非腫瘤領域的研發持續深入,市場對該産品商業化預期也隨之走高。
在此背景下,亞盛醫藥全球産業基地獲發A證,顯示公司作爲持有人不僅對包括重磅産品APG-2575在內的創新藥研發和豐富管線的打造有充分信心,而且對自建工廠作爲全球基地提供符合國際標准的高質量商業化生産能力的強大決心。
上市一周年,耐立克®不斷得到市場驗證
近2個月以來,在港股大盤和生物醫藥板塊不斷波動和回調的背景下,亞盛醫藥股價一路堅挺,期間股價雖有波動,但股價走勢整體趨勢向上,甚至區間最高漲幅超過80%,充分體現公司內在價值正在加速釋放。
市場之所以反饋積極,不僅在于亞盛醫藥進展順利的在研管線,還在于其上市一周年並不斷得到市場驗證的核心産品耐立克®。
智通財經APP了解到,上市一年來,耐立克®的臨床數據不斷得到驗證,已成爲廣大血液科醫生戰勝“耐藥“的武器。
早在今年上半年,耐立克®就獲中國臨床腫瘤學會(CSCO)指南和中國抗癌協會《中國腫瘤整合診治指南(CACA)》推薦,治療伴有T315I突變的既往TKI耐藥慢粒患者(CACA指南亦推薦該品種用于治療接受過2種以上TKI耐藥或不耐受的慢粒患者)。
在提升耐立克®的市場可及性和患者可負擔性方面,截至2022年10月底,耐立克已獲得52個城市、15個省份的惠民保報銷資格。
作爲一款具備全球best-in-class潛力的叁代TKI重磅産品,耐立克®不僅在中國填補了臨床無藥可醫的空白,在國際學界和市場同樣獲得雙重期待和好評。
目前,耐立克共獲1項美國食品藥品監督管理局(FDA)快速通道資格、4項FDA孤兒藥資格認定和1項歐洲藥品管理局(EMA)的歐盟孤兒藥資格認定。
值得投資者注意的是,爲了讓全球患者盡早獲益,亞盛醫藥于今年7月與爲全球制藥企業提供專業供藥解決方案的服務商——Tanner Pharma集團攜手,啓動一項創新的指定患者藥物使用計劃(NPP)。
該項目將在耐立克®尚未獲得上市許可的區域爲指定患者提供使用該藥物的機會,計劃覆蓋100多個國家和地區,以可靠、負責、符合倫理規範和當地法規的方式將耐立克®帶給衆多無藥可醫的慢粒患者。
與此同時,耐立克®在海外的臨床研究也在緊鑼密鼓的進行中。在今年亞盛醫藥入選ASH年會口頭報告的4項臨床階段研究數據中,便包括耐立克®的3項臨床進展,並且其中1項爲其首次公布的美國臨床研究數據。
以上足以說明,亞盛醫藥在核心産品的研發及商業化領域已實現了長足進步,而此次全球産業基地的正式啓動,更意味着亞盛醫藥可滿足新藥從臨床前到臨床、從IND到NDA、再到商業化的全鏈條的研發和生産需要,進一步提升市場對于其整體産品管線順利商業化落地和市場拓展的信心,推動公司估值曲線進一步向上攀升。