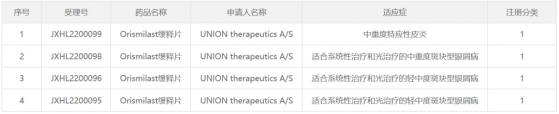
智通財經APP獲悉,7月25日,中國國家藥品監督管理局藥品審評中心(CDE)官網公示,一款名爲orismilast緩釋片的1類新藥已獲得多項臨床試驗默示許可,擬開發用于中重度特應性皮炎,以及適合系統性治療和光治療的中重度斑塊型銀屑病。公開資料顯示,orismilast是UNION公司開發的一款下一代PDE4抑制劑,已獲得美國FDA授予快速通道資格。2021年,信達生物(01801)通過一項超2.6億美元的合作獲得了該候選藥在中國(包括中國大陸、香港、澳門和台灣地區)的獨家授權。
據悉,orismilast是一種強效和高選擇性的下一代PDE4抑制劑,具有廣泛的抗炎特性。該藥由LEO Pharma開發,並于2020年被UNION公司獲得。2021年9月,信達生物宣布與UNION公司達成一項獨家授權協議。根據協議條款,信達生物將獲得orismilast在中國的研究、開發和商業化獨家權益。UNION公司將收到2000萬美元的首付款,並有權獲得累計不超過2.47億美元的裏程碑付款,以及orismilast在中國年度銷售淨額的特許權使用費。同時,UNION公司保留orismilast在除中國以外的全球其它地區的權益。
該公司基于orismilast開發了兩個候選産品,目前均處于2期臨床研究階段:其中,UNI50001是一種口服PDE4抑制劑,擬開發用于治療銀屑病、特應性皮炎和化膿性皮炎;UNI50002是orismilast的外敷制劑,擬開發用于治療特應性皮炎。
目前orismilast緩釋片正在開展多項2期臨床試驗,針對適應症包括中度至重度特應性皮炎、中度至重度斑塊型銀屑病、輕度至重度化膿性汗腺炎等。此次該産品在中國獲批臨床,意味着該産品也即將在中國進入臨床開發階段。