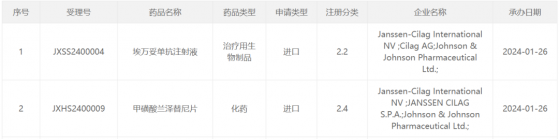
智通財經APP獲悉,1月26日,中國國家藥監局藥品審評中心(CDE)官網公示,強生(JNJ.US)兩款產品上市申請獲得受理,分別爲EGFR/MET雙特異性抗體療法埃萬妥單抗注射液(amivantamab)和第三代EGFR-TKI口服藥物甲磺酸蘭澤替尼片(lazertinib)。
資料顯示,埃萬妥單抗是強生旗下強生創新制藥開發的一款靶向EGFR和MET的在研全人源化雙特異性抗體,它除了能夠阻斷EGFR和MET介導的信號傳導以外,還可以引導免疫細胞靶向攜帶激活性和抗性EGFR/MET突變和擴增的腫瘤。2021年5月,該產品獲得美國FDA正式批准,用於治療鉑類化療期間或之後進展的EGFR外顯子20插入突變非小細胞肺癌(NSCLC)患者。2023年8月,該產品還向FDA遞交了補充生物製品許可申請(sBLA),與化療聯用一線治療攜帶EGFR外顯子20插入突變的局部晚期或轉移性NSCLC患者。
在中國,埃萬妥單抗曾被CDE納入突破性治療品種,用於治療含鉑雙藥化療期間或之後進展,或對含鉑化療不耐受的EGFR 20號外顯子插入突變的轉移性或手術不可切除的NSCLC患者。2023年10月,該產品上市申請獲得CDE受理。本次是該產品在中國遞交的第二項上市申請。