隨着全球人口老齡化的不斷加劇,帶狀疱疹日益成爲了影響老年人生活質量的疾病,預防老年人罹患帶狀疱疹的疫苗也逐漸成爲了增進民衆健康的不二之選。
根據弗若斯特沙利文數據,按銷售收入計算,中國帶狀疱疹疫苗市場有望在2030年迎來285億的大市場。目前國內帶狀疱疹疫苗市場是雙寡頭格局,只有GSK的Shingrix®和百克生物的感維®獲批上市。
智通財經APP注意到,該賽道的資本市場新貴綠竹生物-B(02480.HK)也參與了帶狀疱疹疫苗研發,從研發進度和技術路徑來看,綠竹生物是國內重組帶疱疫苗臨床進展最快、已披露數據最好的一家,競爭潛力不容小觑。
公開資料顯示,綠竹生物已在9月28日宣布正式啓動重組帶狀疱疹疫苗LZ901的叁期臨床研究,該疫苗也是除Shingrix®外全球第二家進入叁期臨床研究的重組帶狀疱疹疫苗。若綠竹生物産品最終上市,將帶給市場多大的沖擊?本文將從技術路線、臨床進度、臨床數據、出海情況等方面來進行分析。
技術路線:重組蛋白路線保護率更優
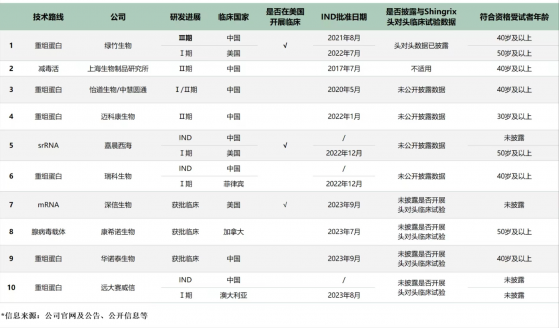
重組疫苗、減毒活疫苗與RNA疫苗,是目前帶狀疱疹疫苗研發的叁條主流技術路線。
最早上市的減毒活疫苗,由于其較低的保護效率、較短的保護期限,逐漸被重組蛋白疫苗所替代。而RNA技術路線的帶狀疱疹疫苗,由于其新技術面世時間不長,仍需長時間驗證。
重組帶狀疱疹疫苗的主流地位從兩方面表現:其一,Shingrix®壟斷全球市場,在其上市後第叁年(即2020年11月),減毒疫苗Zostavax®不再于美國售賣。2022年,Shingrix®在全球的銷售額約爲36億美元。2023年,GSK披露第二季度財報顯示,Shingrix®銷售額同比增長20%,僅半年時間就銷售高達約22億美元。其二,目前處于臨床階段的其他在研的帶狀疱疹疫苗大都選擇重組蛋白路線,說明其市場認可程度高。
臨床進度:綠竹生物斷檔式領先
從國內公司競爭格局來看,綠竹生物的技術路線是重組蛋白路線,已于2023年9月進入叁期臨床研究,研發進度斷檔式領先。
據綠竹生物9月28日公告披露,其已于江蘇、山東、湖北和山西等四個省份啓動了其核心産品LZ901的多中心、隨機、雙盲、安慰劑對照設計,用于評價在40歲及以上成人中預防帶狀疱疹保護效力、安全性的叁期臨床試驗,總入組規模約2.6萬人,截至公告日已完成首批受試者入組。
臨床數據:安全性和免疫原性優秀
LZ901是綠竹生物自主研發的在研重組帶狀疱疹疫苗及核心産品,爲全球首款具有四聚體分子結構的帶狀疱疹疫苗。
與天然存在的VZV抗原相比,其分子結構具有雙倍的Fc區供抗原呈遞細胞(APC)結合,LZ901主動向免疫細胞呈遞VZV抗原以觸發免疫反應。此外,LZ901在臨床前研究中表現出高免疫原性和安全性,同時誘導出特異性體液和細胞免疫。
與Shingrix®相比,LZ901的具備以下優勢:
首先,副作用小。誠如LZ901在中國的一期和二期臨床試驗安全性數據證明,施用LZ901的受試者的一級至叁級AE的總體數量和發生率均遠低于施用Shingrix®的受試者。且Shingrix®海外叁期臨床數據顯示其總體叁級不良反應率超過20%,而LZ901目前二期臨床數據顯示其疫苗組叁級不良反應率僅爲1%。
此外,該公司采用的劑型爲方便易用的液體制劑。綠竹生物在研重組帶狀疱疹疫苗LZ901采用了高度穩定的液體制劑配方,可以方便地儲存和運輸。它在37˚C下可穩定兩周,在25˚C下穩定12周,在2-8˚C下可穩定的存放24個月以上。由于液體制劑只含有常規使用的氫氧化鋁佐劑,不含免疫刺激物,減少了注射部位發生嚴重不良反應的可能性,因此,施用LZ901的副作用很小。
其次,強保護。根據從LZ901在中國的一期臨床試驗所收集的免疫原性數據,其證明與Shingrix®相比,在全程接種LZ901後,抗VZV抗體水平並無顯著差異。而且,LZ901誘導更強細胞免疫反應,對帶狀疱疹應有很強的保護作用。在人體頭對頭試驗中,與Shingrix®相比,LZ901誘導更強的細胞免疫反應,輔助T細胞(CD4+)及細胞毒性T細胞(CD8+)表達多種類型的免疫細胞啓動生物標志物的細胞比例更高。這表明LZ901在誘導細胞免疫方面不弱于Shingrix®,LZ901提供強大的帶狀疱疹保護。
值得一提的是,LZ901定價更具競爭力。與Shingrix®全程接種約3200元的定價相比,LZ901的定價將更適合中國國情,更具有性價比。國內按照批簽發口徑計算GSK帶狀疱疹疫苗滲透率僅爲0.3%左右,滲透率提升空間較大。
出海情況:第一家中美同時臨床的疫苗 兩地上市增量空間可期
在出海大趨勢下,國內創新藥企們陸續嘗試了海外授權(license out)等多種出海模式。隨着出海經驗積累,在中美兩地同時展開臨床試驗這一新模式逐漸在創新藥企中流行。
今年2月,綠竹生物在美國紐約啓動重組帶狀疱疹疫苗LZ901的一期臨床研究,是該賽道內國內首個在中美兩地同時進行臨床研究的企業。到目前爲止,也仍然是唯一獲得FDA批准臨床的國産重組帶疱疫苗。
同時據綠竹生物9月28日的公告披露,其近日已于日本取得LZ901的發明專利注冊。除美國、歐洲、英國、韓國、加拿大、澳大利亞的在申請專利外,綠竹生物已獲得中國、俄羅斯和日本的專利批准。
智通財經APP認爲,綠竹生物加速出海,是順應行業發展趨勢的舉措,也是國産疫苗創新的一個重大裏程碑。一方面,國內的醫保定價體系正在倒逼創新藥企出海以獲取更大利潤空間;另一方面,Biotech企業們要打開估值空間,出海也是必然要走的路徑。而企業一旦決心要出海,作爲全球最大醫藥市場的美國必然是繞不過去的。因此,綠竹生物作爲出海先行者,反映了綠竹生物是以全球藥物開發的視角來研發藥物,更表露出其全球化布局的雄心。
若能順利在全球市場上市,綠竹生物的增量空間值得期待。以Shingrix®爲例,帶狀疱疹疫苗Shingrix® 2022年全年實現銷售收入36億美元,中國、德國市場同比增長超過100%,刷新了自上市來的銷售記錄。GSK認爲Shingrix®在2026年的銷售收入有望超過40億英鎊。
綠竹生物重組帶疱疫苗臨床進展再進一步,則意味着其研發穩步推進,産品向市場化腳步加快。此外,公司産品不僅效果出衆且價格極具競爭力,若順利上市,將顛覆這一産業競爭格局。創新藥的投資邏輯在于技術卡位,從這一點來看,綠竹生物的價值巨大。