最近兩個月,傳奇生物(LEGN.US)過的並不算平靜。
先是在4月19日,公司股價因前一日核心産品臨床數據泄露大漲近20%,公司被迫提前完成2億美元融資;再是Q1財報披露,核心産品Carvykti商業化上市後首個完整年的銷售額出爐,放量明顯。
本來在3月10日,傳奇生物股價已經下探到階段性低點的42.91美元,但幾經催化下,其股價在5月15日已經來到最高73.30美元,區間漲幅達到70.82%。而其中繞不開的一個關鍵點就是其首款商業化産品Carvykti。
超預期臨床表現或引發“賽道地震”
關于此輪傳奇生物的股價啓動,主要源于Carvykti最新臨床數據的提前泄露。
智通財經APP了解到,在一份EHA會議摘要中,傳奇生物BCMA CAR-T療法3期臨床CARTUDE-4的數據表示,Carvykti(西達基奧侖賽)可以降低74%的疾病進展或死亡風險。
關于CARTITUDE-4研究,這是一項國際、隨機、開放標簽的3期研究,用于評估CAR-T療法與泊馬度胺、硼替佐米和地塞米松(PVd)或達雷木單抗、泊馬度胺和地塞米松(DPd)在既往接受過一到叁線治療的複發和來那度胺難治性多發性骨髓瘤成人患者中的療效和安全性。
試驗結果顯示,在既往有1-3次LOT(lines of therapy)的來那度胺難治性患者中,相比于SOC單次cilta-cel輸注顯著改善了PFS,在患者群體中具有良好的獲益/風險狀況,疾病進展/死亡減少74%,CR和MRD陰性率高,這突出表明cilta-cel有可能成爲多發性骨髓瘤患者首次複發後的關鍵療法。
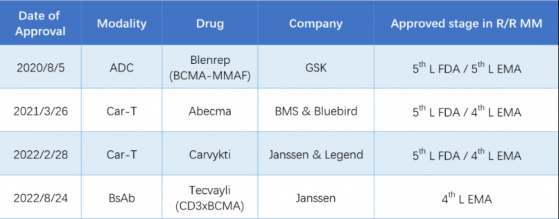
值得一提的是,西達基奧侖賽此前在美國FDA獲批用于治療複發或難治性多發性骨髓瘤成人患者,這些患者既往接受過至少四線治療,也就是說其獲批的是五線治療的適應症。
但此次CARTUDE-4臨床研究針對的則是更前線的2-4線治療(經過1-3線治療),臨床試驗獲得的積極結果。加上目前BCMA CAR-T療法在治療多發性骨髓瘤領域的潛力較大且已被多個國家認可和批准,這爲傳奇生物的BCMA CAR-T産品在全球範圍內的推廣提供了廣闊的市場空間,或將直接攪動細分賽道的競爭格局。
此前,BMS研發的BCMA CAR-T産品Abecma在2021年3月獲得美國FDA批准上市,是全球首款獲批上市的BCMA CAR-T産品。2022年,Abecma的銷售額達到3.88億美元,同比增長達到136%。年銷售額已超過部分更早上市的CD19靶點CAR-T産品,躍居榜叁。並且根據今年2月公布的數據,在RRMM患者中,Abecma可降低2-4線MM患者51%的疾病進展或死亡風險。
雖然目前Abecma和Carvykti二者之間並沒有“頭對頭”的臨床數據,但憑借表現優異的CARTUDE-4臨床結果,Carvykti顯然有與Abecma掰手腕的資格。
另外,在CARTUDE-4臨床結果披露後,傳奇生物Q1財報與2022年年報的信息價值也隨之水漲船高。
對比Abecma和Carvykti兩款産品的2022年銷售情況,上文提到,Abecma全年營收3.88億美元,而Carvykti的2022年2月28日獲批,全年營收達到1.34億美元,其中二、叁、四季度銷售分別爲0.24億美元、0.55億美元、0.55億美元。而據強生發布的2023年Q1財報顯示,Carvykti在2023年Q1的銷售額爲7200萬美元,銷售額增速明顯,且由此可以計算出Carvykti商業化上市後首個完整年的銷售額爲2.06億美元。
強生曾表示爲Carvykti規劃了50億美元銷售額的産能,一旦後續産能實現規模增長,依托優異臨床數據,傳奇生物將從Carvykti進一步增長的銷售額中獲得更多的分成營收。
不過,由于此次CARTUDE-4臨床結果是被發至EHA官網的臨床數據摘要泄露,還是給公司帶來了一點“小麻煩”。
據悉,傳奇生物原本正在憑借該臨床數據與投資者接洽以募集資金,但在數據泄露後的當晚,傳奇生物母公司卻發布公告,宣布傳奇生物與投資者已完成認購協議的簽訂,以26.12美元的認購價募集了約2億美元。
不懼與雙抗“搶食”
雖然不論從産能規劃還是銷售推廣來看,有強生的助力,傳奇生物後續似乎能“坐等收錢”,但實際上,同樣在4或5線治療複發/難治性多發性骨髓瘤(R/R MM)適應症上,強生除了與傳奇生物共同推出了Carvykti,還與楊森制藥推出了針對同適應症的全球首款靶向BCMA/CD3雙抗Tecvayli。
雙向下注的強生也因此將Carvykti推向了與雙抗搶奪同適應症市場的時代。
去年11月,Tecvayli獲FDA批准上市。其是一款首創的(first-in-class)BCMA/CD3雙特異性T細胞結合抗體,能夠靶向結合T細胞表面表達的CD3受體以及多發性骨髓瘤(MM)細胞和一些健康B系細胞表面表達的B細胞成熟抗原(BCMA)。CD3參與激活T細胞,BCMA在MM細胞上表達水平顯著升高。
Tecvayli得以獲批上市,主要基于其關鍵1/2期MajesTEC-1研究的結果。
數據顯示,Tecvayli治療的總緩解率(ORR)爲61.8%;其中28.2%的患者達到完全緩解(CR)或更好緩解(CR或嚴格的完全緩解[sCR]);在病情緩解的患者中,從治療到首次確認緩解的中位時間爲1.2個月。中位隨訪時間爲7.4個月,中位緩解持續時間(DOR)尚未達到,估計的6個月時DOR率爲90.6%,估計的9個月DOR率爲66.5%。
其實,與其說強生投資的是某款産品,倒不如說是在投資BCMA這個靶點。
據研究發現,BCMA過度表達和激活,在無論是新診斷還是複發的病人中都存在,使得BCMA成爲R/R MM藥物開發的一個高潛力靶標。而不論是早期的Abecma還是Carvykti和Tecvayli,在有效性上都驗證了這一點,並且雙抗Tecvayli,已在響應率(ORR、CR)方面媲美Abecma。
據不完全統計,目前在研的BCMA/CD3 雙抗約17種。而根據Fortune Business Insights的報告,2018年全球多發性骨髓瘤市場規模爲約195億美元,預計到2026年將達到約310億美元,預測期間年複合增長率將爲6.0%。在如此龐大的市場規模和臨床需求下,具有“現貨”性質的雙抗Tecvayli顯然有望與需要長時間制備CAR-T藥物形成競爭。
不過從目前的銷售力度和産品研發情況來看,強生對CAR-T的偏好其實更大。原因之一在于,當下鮮有Bigpharm在BCMA CAR-T上有成熟的布局,強生能夠在該領域做到更爲深度的市場擴張;另一方面,隨着Carvykti用于MM早期治療的臨床研究數據的披露,後續Carvykti有望布局更前線的2-4線治療,而與Tecvayli形成差異化競爭局面,因此從投資者角度來看,當下時間節點加碼估值剛剛啓動的傳奇生物和Carvykti無疑是個非常具有吸引力的選擇。